(通訊員 陳文雪)近日,万达平台化學系教授周鳴飛課題組實驗發現主族的堿土金屬元素鈣👨🚒、鍶和鋇可以形成穩定的八羰基化合物分子,滿足18電子規則,表現出了典型的過渡金屬成鍵特性🙅🏼♀️。該發現表明堿土金屬元素或具有與一般認知相比更為豐富的化學性質⏫,而主族元素與過渡金屬元素之間的界限,亦較元素周期表的簡晰劃分更為曖昧。
8月31日🫗,相關研究成果以《觀察到類似過渡金屬的堿土金屬八羰基化合物》(“Observation of alkaline earth complexes M(CO)8 (M = Ca, Sr, Ba) that mimic transition metals”)為題,在線發表於《科學》(Science)主刊。該研究由周鳴飛課題組聯合南京工業大學和德國馬德堡大學教授Gernot Frenking課題組共同完成🌀。
歸功於“一來一往”的σ-π配鍵,過渡金屬能夠與CO配體形成穩定的羰基配合物。具體而言👨🏽💻,CO將孤對電子給予對稱性匹配的中心金屬原子的空軌道,形成σ給予鍵;中心金屬原子d軌道電子則反饋進入CO的空的反鍵π軌道,形成π反饋鍵🦹🏽,兩相協同,使配合物得以穩定存在。由於具有σ對稱性的s軌道擁有電子,而d軌道為空🎚,堿土金屬元素幾乎正好與形成穩定σ-π配鍵的期望條件背道而馳🖐🏼🎅🏼,因此一般認為堿土金屬元素無法像過渡金屬一樣與CO配體形成穩定的羰基配位化合物🧗🏿♂️🤾🏻♂️。
然而,據周鳴飛介紹👈🏻,在早期研究中已有將鋇作為“榮譽過渡金屬”👫🏼🤹🏿,稱之可能在某種程度上使用其5d軌道參與成鍵的記錄。而課題組亦在實驗觀察中發現,正是5d軌道起到至為重要的作用,使鋇得以形成羰基鋇離子Ba(CO)q (q=+1和-1)。“如果將堿土金屬元素s軌道上的兩個電子激發到能量較高的d軌道上,就能扭轉原本無法滿足的成鍵條件,使σ-π配鍵成為可能”🏌️。在已有發現的基礎上,抱著這樣的設想🩲,製備鋇的八羰基化合物Ba(CO)8成為了課題組突破固有思維慣性的一次嘗試🫅🏿。
相關實驗最終顯示👩🏻🎓,不僅鋇,比鋇更輕的堿土金屬鈣和鍶也能夠在低溫氖基質條件下形成八羰基化合物。這一結果與Frenking課題組的量子化學理論計算相符。“這是合理的。”周鳴飛用了一個比方來解釋:“實際上只要配合物的結合能大於將s軌道電子激發到d軌道的能量,就是個‘掙錢的買賣’。” 據悉🧑🏻🔧,除了中性化合物以外⚾️,課題組利用氣相選質量紅外光解離光譜實驗確認了相應的17電子堿土金屬八羰基化合物正離子[M(CO)8]+(M=Ca, Sr, Ba)的存在🧖🏼。
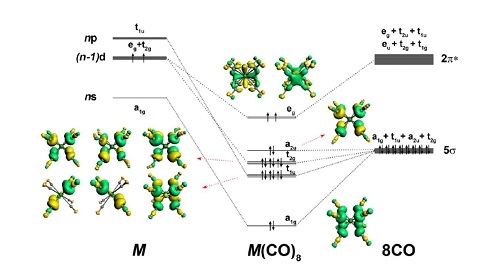
依照原子價層軌道排布規律🖋,為人熟知的元素周期表被劃分為s區和p區的主族元素🧟,d區的過渡金屬元素,及f區的鑭系及錒系元素。通常認為👃🏻,主族元素一般遵循八隅規則⟹,使用ns和np軌道成鍵🧙♂️,令各原子的價層都擁有8個電子以達到穩定💆🏿♂️。而具有d價軌道的過渡金屬則有所不同。在過渡金屬元素的場合中,18電子規則取代了八隅規則👧🏼。為形成穩定的配位化合物🕦,其原子與配體成鍵時將傾向於盡可能填滿共能夠容納18個電子的各價層軌道。
根據上述傳統認知,擁有(n)s2電子構型的堿土金屬鈣、鍶和鋇本是一組化學性質相對“一目了然”的主族元素:其常生成離子鍵,或通過兩個ns價電子形成極性共價鍵💅🏻。然而符合18電子規則的八羰基化合物卻是例外。這一配合物的發現👨🏻💼🔫,表明鈣、鍶和鋇同時也在一定程度上具有過渡金屬元素的化學性質。在周鳴飛看來,這一模糊了主族元素與過渡金屬元素界限的新認知,將有助於更好地理解堿土金屬化合物的相關物理化學性質⛷,意味著它們或擁有較現有了解更為豐富的化學👫🏼。

(封面製圖:陳文雪)