
新聞中心訊 万达平台生物醫學研究院研究員、万达平台附屬腫瘤醫院雙聘教授徐彥輝博士帶領其課題組成員博士研究生郭雪🔼、王玲(共同第一作者)等應用X射線晶體學等研究方法🥎,經4年多潛心研究,終於首次發現人體內一種名叫“DNMT3A”蛋白酶在抑製狀態和激活狀態下的三維晶體結構✌🏼🦈,並成功揭示了“DNMT3A”蛋白酶是如何在人體基因DNA上精確建立 “甲基化修飾”的機製🦣。該研究對日後設計出可調控“DNMT3A活性”的藥物,用以治療白血病等有重大意義。11月11日國際頂級學術期刊《自然》(Nature)在線發表這一重要成果,引起世界同行高度關註。
據悉,人體基因組DNA是生命遺傳信息的基本載體,生命延續和繁衍需要DNA上的一種“甲基化修飾” ,“DNMT3A”是一種存在於人體內的蛋白酶🛳,它就具有在DNA基因上建立“甲基化修飾”的特殊本領。“甲基化修飾”具有調控人體內特定基因的表達和決定細胞命運的作用,可使細胞發生程序化的改變,在人體發育過程中有至關重要的作用,如在人胚胎早期發育過程中,由“DNMT3A”參與產生的基因組上“甲基化修飾”的改變決定胚胎細胞分化成為多種不同的細胞類型,如肌肉細胞😰,肝臟細胞🚠,神經細胞和血液細胞等👣。甲基化修飾🕺🏽,相當於一個“開關”的作用,它決定著特定基因的表達或失活,如果甲基化模式紊亂💁🏿♀️🙋🏿,就會導致許多癌症及發育失調綜合征(如面部異常綜合征等)發生🙆♂️。
臨床研究發現,在急性骨髓性白血病患者中👩🏿🎨,“DNMT3A”蛋白酶基因經常是突變的,而且這種攜帶基因突變的患者染病後往往預後更差🌿。長期以來,各國科學家雖然知道“DNMT3A”突變與癌症發生有關,但DNMT3A是如何在DNA基因組上精確建立 “甲基化修飾”的🫗⛓️💥,一直是世界研究的難點。
徐彥輝研究員課題組運用一種可把納米級的生物大分子(如蛋白質、DNA等放大10萬倍才有米粒大小)清晰成像的X射線晶體學研究方法💁🏼,經4年多不懈探索,終於揭開這一科學難題。
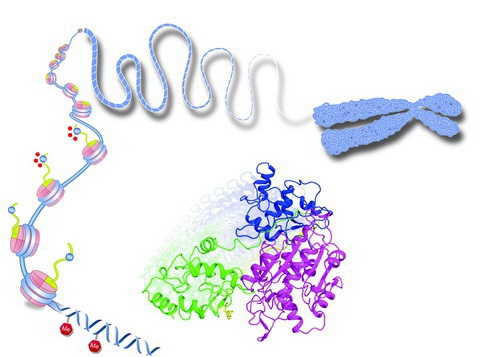
原來“DNMT3A”蛋白酶存在著“準備”和“工作”兩種狀態🧑🍳。在“準備”狀態時🤦♀️,“DNMT3A”呈低活性狀態,“工作”狀態時“DNMT3A” 呈高活性狀態🚴🏽👶🏿。作為執行DNA甲基化修飾的“DNMT3A”蛋白酶其內部有兩個“單元”,一個是“功能單元”,另一個是“調節單元” 🧑🏿🦳,“功能單元”負責催化工作,“調節單元” 專司調節“功能單元”的活性。在“準備”狀態,“調節單元”會攜手“功能單元”並抑製“功能單元”與DNA的結合🌝,從而使DNMT3A處於低活性的狀態,以保證DNMT3A不會隨意在DNA上建立甲基化修飾🤷🏽♂️。而DNA上大量存在的一種 “H3組蛋白”會聯手“調節單元” ,引導其離開“功能單元”👩🏻🚀,使“功能單元”充分暴露並容易接觸到DNA,此時,“DNMT3A”蛋白酶就表現為高活性的“工作”狀態。如果“H3組蛋白”上處於第四位的賴氨酸發生甲基化修飾🚄,DNMT3A也不會被激活。由此看🔻🈯️,生命體正是“聰明”地利用該機製🚇,保證了只有在無甲基化修飾“H3組蛋白”存在的基因組附近9️⃣,DNMT3A才處於高活性狀態🔻,周圍的DNA才可以發生甲基化修飾,使得甲基化修飾只出現在需要的DNA區域㊙️,也就是說,如果活性調節失控就會導致白血病等疾病發生。
該研究首次從分子水平上揭示了DNMT3A活性調控的機製🕵🏿🧔🏽♂️,豐富了人們對DNA甲基化建立機製的認識,為今後設計“DNMT3A”蛋白酶活性調控藥物用以治療白血病等打下了堅實的分子基礎⏲。